Реакции в виде озноба, боли в ротоглотке, тошноты: что указано в инструкции к вакцине "Спутник V"
Опубликовано:

С 1 февраля в Казахстане стартовала массовая вакцинация от коронавируса – прививать людей начали российской вакциной «Спутник V». В первые дни вакцинации журналисты NUR.KZ попросили медиков показать нам вакцину и полную аннотацию препарата, чтобы изучить всю описанную там информацию.
"Не трясти": точное название вакцины и требования к хранению
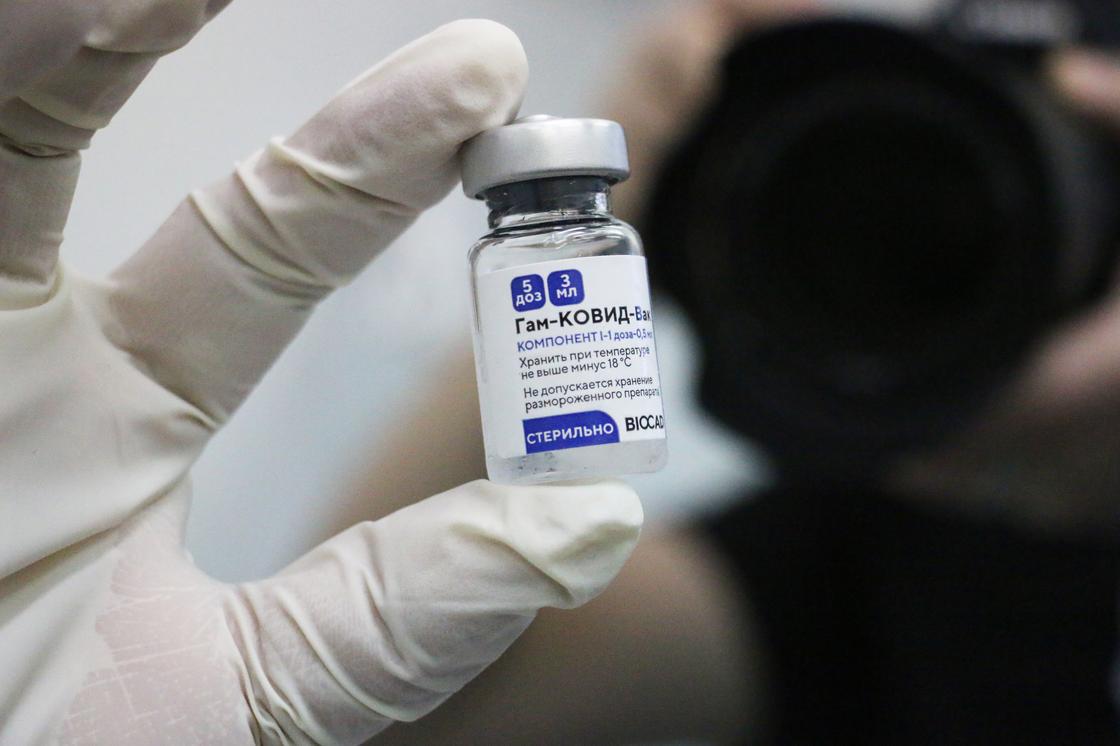
На упаковке вакцины указано название «Гам-КОВИД-Вак» - комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом Sars-CoV-2 (новой коронавирусной инфекции Covid-19).
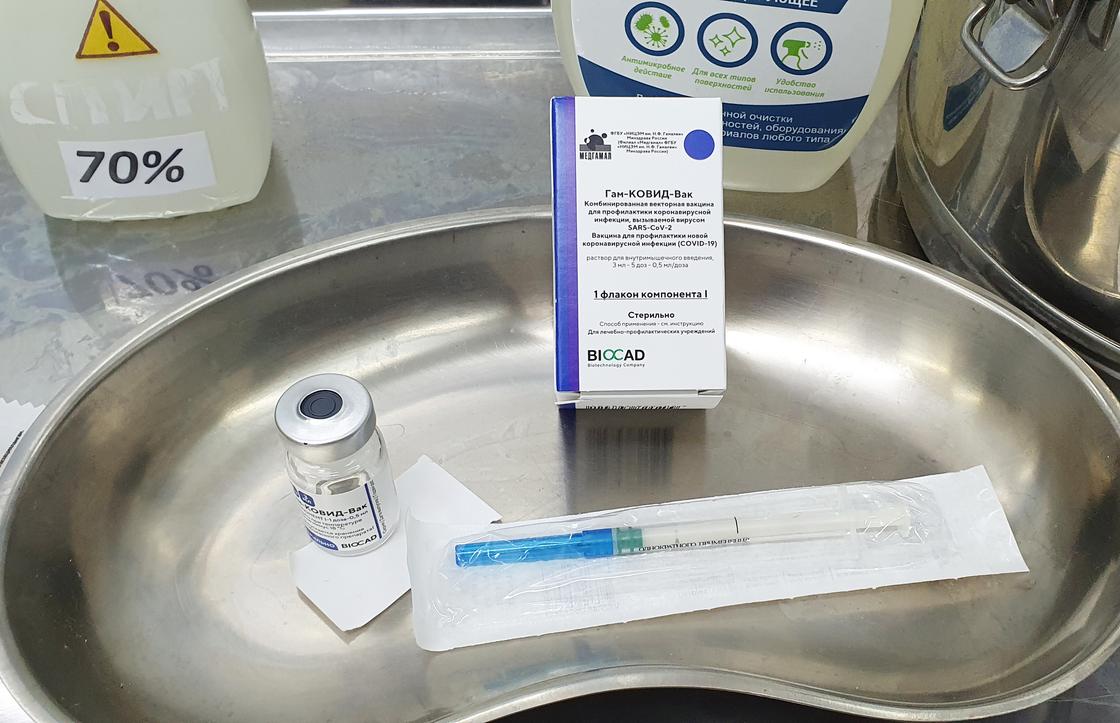
Мы сфотографировали упаковку и флакон компонента 1 – это первая «часть» вакцины, компонент 2 вводится пациенту через 21 день.
Вводят строго внутримышечно в верхнюю треть плеча либо латеральную широкую мышцу бедра – введение в вену строго запрещено.

При нас флакон достали из холодильника, он был заморожен – медик должен дождаться его полной разморозки при комнатной температуре.
Остаток включений льда не допускается, трясти флакон запрещено – перемешивать содержимое можно только «покачиванием».
Температура хранения - не выше минус 18-ти градусов.
Производитель: АО "ГЕНЕРИУМ", Россия, Владимирская область.
Привить 5 человек за 2 часа
Во флаконе 3 мл вещества – это 5 доз по 0,5 мл.
После разморозки хранить флакон можно не более 2-х часов – повторная заморозка запрещена. Это значит, что в течение 2-х часов медик должен привить 5 человек либо утилизировать остатки препарата.
Состав вакцины – компонент 1 и компонент 2
Действующее вещество компонента 1: рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2.
Действующее вещество компонента 2: рекомбинантный аденовирусный вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Вспомогательные вещества обоих компонентов: трис (гидроксиметил), аминометан, натрия хлорид, сахароза, полисорбат 80, магния хлорида гексагидрат, ЭДТА динатриевая соль дигидрат, этанол 95%, вода для инъекций.

Первые строки в инструкции к вакцине гласят:
"Данный препарат зарегистрирован по процедуре регистрации препаратов для применения в условиях угрозы возникновения, возникновения и ликвидации ЧС.
Инструкция подготовлена на основании ограниченного объема клинических данных и будет дополняться по мере поступления новых данных".
Противопоказания
- гиперчувствительность к какому-либо компоненту вакцины или вакцины, содержащей аналогичные компоненты,
- тяжелые аллергические реакции в анамнезе,
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ – вакцинацию проводят после нормализации температуры,
- беременность и период грудного вскармливания,
- возраст до 18-ти лет (в связи с отсутствием данных об эффективности и безопасности),
Противопоказания для введения компонента 2: тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура 40 градусов и т.д) на введение компонента 1.
Препарат применять с осторожностью при:
- хронические заболевания печени и почек,
- эндокринные заболевания (нарушение функции щитовидной железы и сахарный диабет в стадии декомпенсации),
- тяжелые заболевания системы кроветворения,
- эпилепсии и другие заболевания ЦНС,
- острый коронарный синдром и острое нарушение мозгового кровообращения,
- миокардит, эндокардит, перикардит.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп населения:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний),
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Взаимодействие с другими препаратами – исследования не проводились.
Особенности влияния на управление транспортным средством – исследования не проводились.

Нежелательные реакции на вакцину
Нежелательные реакции могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней.
Часто: непродолжительный гриппоподобный синдром с ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью.
Также боль в ротоглотке, заложенность носа, першение в горле, ринорея, тошнота, рвота, снижение аппетита, диспепсия.
Местные реакции в виде болезненности в месте введения, с гиперемией, отечностью, зудом.
Иногда: увеличение регионарных лимфоузлов, у некоторых возможны аллергия, кратковременные повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
Редко: головокружения и обмороки.
Организация, принимающая претензии по качеству лекарственных средств, а также ответственная за пострегистрационное наблюдение за безопасностью вакцины в Казахстане - Карагандинский фармацевтический комплекс.


- Дарига Назарбаева планирует сделать прививку от коронавируса российской вакциной
- Иммунолог развеял "вредные" мифы о прививках против COVID-19
Нашли ошибку в публикации? Сообщите нам об этом.
Оригинал статьи: https://www.nur.kz/health/coronavirus/1896951-reakcii-v-vide-oznoba-boli-v-rotoglotke-tosnoty-cto-ukazano-v-instrukcii-k-vakcine-sputnik-v/
